Hno3 какой электролит. Учебная книга по химии
Таких электролитов близка к 1.
К сильным электролитам относятся многие неорганические соли , некоторые неорганические кислоты и основания в водных растворах, а также в растворителях, обладающих высокой диссоциирующей способностью (спирты , амиды и др.).
Wikimedia Foundation . 2010 .
Смотреть что такое "Сильные электролиты" в других словарях:
сильные электролиты - – электролиты, которые в водных растворах практически полностью диссоциированы. Общая химия: учебник / А. В. Жолнин … Химические термины
Вещества, обладающие ионной проводимостью; их называют проводниками второго рода прохождение тока через них сопровождается переносом вещества. К электролитам относятся расплавы солей, оксидов или гидроксидов, а также (что встречается значительно… … Энциклопедия Кольера
Электролиты - жидкие или твердые вещества, в которых в результате электролитической диссоциации образуются в сколько нибудь заметной концентрации ионы, обусловливающие прохождение постоянного электрического тока. Электролиты в растворах… … Энциклопедический словарь по металлургии
Электролит химический термин, обозначающий вещество, расплав или раствор которого проводит электрический ток вследствие диссоциации на ионы. Примерами электролитов могут служить кислоты, соли и основания. Электролиты проводники второго рода,… … Википедия
В широком смысле жидкие или твёрдые в ва и системы, в к рых присутствуют в заметной концентрации ионы, обусловливающие прохождение по ним электрич. тока (ионную проводимость); в узком смысле в ва, распадающиеся в р ре на ионы. При растворении Э.… … Физическая энциклопедия
В ва, в к рых в заметной концентрации присутствуют ионы, обусловливающие прохождение электрич. тока (ионную проводимость). Э. также наз. проводниками второго рода. В узком смысле слова Э. в ва, молекулы к рых в р ре вследствие электролитической… … Химическая энциклопедия
- (от Электро... и греч. lytos разлагаемый, растворимый) жидкие или твёрдые вещества и системы, в которых присутствуют в сколько нибудь заметной концентрации ионы, обусловливающие прохождение электрического тока. В узком смысле Э.… … Большая советская энциклопедия
У этого термина существуют и другие значения, см. Диссоциация. Электролитическая диссоциация процесс распада электролита на ионы при его растворении или плавлении. Содержание 1 Диссоциация в растворах 2 … Википедия
Электролит вещество, расплав или раствор которого проводит электрический ток вследствие диссоциации на ионы, однако само вещество электрический ток не проводит. Примерами электролитов могут служить растворы кислот, солей и оснований.… … Википедия
ДИССОЦИАЦИЯ ЭЛЕКТРОЛИТИЧЕСКАЯ - ДИССОЦИАЦИЯ ЭЛЕКТРОЛИТИЧЕСКАЯ, распад находящихся в растворе электролитов на электрически заряженные ионы. Коеф. вант Гоффа. Вант Гофф (van t Ной) показал,что осмотическое давление раствора равно давлению, к рое производило бы растворенное… … Большая медицинская энциклопедия
Книги
- Явление возврата Ферми-Паста-Улама и его некоторые приложения. Исследование возврата Ферми-Паста-Улама в различных нелинейных средах и разработка генераторов спектра ФПУ для медицины , Березин Андрей. Эта книга будет изготовлена в соответствии с Вашим заказом по технологии Print-on-Demand. Основные результаты работы заключаются в следующем. В рамках системы связанных уравнений Кортевега…
, , 21 , , ,
, 25-26 , 27-28 ,
, 30, , , , , , , , /2003
§ 6.3. Сильные и слабые электролиты
Материал этого раздела частично вам знаком по ранее изученным школьным курсам химии и из предыдущего раздела. Кратко повторим, что вам известно, и познакомимся с новым материалом.
В предыдущем разделе мы обсуждали поведение в
водных растворах некоторых солей и органических
веществ, полностью распадающихся на ионы в
водном растворе.
Имеется ряд простых, но несомненных
доказательств того, что некоторые вещества в
водных растворах распадаются на частицы. Так,
водные растворы серной H 2 SO 4 , азотной HNO 3 ,
хлорной HClO 4 , хлороводородной (соляной) HCl,
уксусной CH 3 COOH и других кислот имеют кислый
вкус. В формулах кислот общей частицей является
атом водорода, и можно предположить, что он (в
виде иона) является причиной одинакового вкуса
всех этих столь различных веществ.
Образующиеся при диссоциации в водном растворе
ионы водорода придают раствору кислый вкус,
поэтому такие вещества и названы кислотами. В
природе только ионы водорода имеют кислый вкус.
Они создают в водном растворе так называемую
кислотную (кислую) среду.
Запомните, когда вы говорите «хлороводород», то имеете в виду газообразное и кристаллическое состояние этого вещества, но для водного раствора следует говорить «раствор хлороводорода», «хлороводородная кислота» или использовать общепринятое название «соляная кислота», хотя состав вещества в любом состоянии выражается одной и той же формулой – НСl.
Водные растворы гидроксидов лития (LiOH), натрия
(NаОН), калия (КОН), бария (Ва(ОН) 2), кальция
(Са(ОН) 2) и других металлов имеют одинаковый
неприятный горько-мыльный вкус и вызывают на
коже рук ощущение скольжения. По-видимому, за это
свойство ответственны гидроксид-ионы ОН – ,
входящие в состав таких соединений.
Хлороводородная HCl, бромоводородная HBr и
йодоводородная HI кислоты реагируют с цинком
одинаково, несмотря на свой различный состав, т.
к. в действительности с цинком реагирует не
кислота:
Zn + 2НСl = ZnСl 2 + Н2,
а ионы водорода:
Zn + 2H + = Zn 2+ + Н 2 ,
и образуются газообразный водород и ионы цинка.
Смешивание некоторых растворов солей, например
хлорида калия KCl и нитрата натрия NaNO 3 , не
сопровождается заметным тепловым эффектом, хотя
после выпаривания раствора образуется смесь
кристаллов четырех веществ: исходных – хлорида
калия и нитрата натрия – и новых – нитрата калия
КNO 3 и хлорида натрия NaCl. Можно предположить,
что в растворе две исходные соли полностью
распадаются на ионы, которые при его выпаривании
образуют четыре кристаллических вещества:
Сопоставляя эти сведения с
электропроводностью водных растворов кислот,
гидроксидов и солей и с рядом других положений,
С.А.Аррениус в 1887 г. выдвинул гипотезу
электролитической диссоциации, согласно которой
молекулы кислот, гидроксидов и солей при
растворении их в воде диссоциируют на ионы.
Изучение продуктов электролиза позволяет
приписать ионам положительные или отрицательные
заряды. Очевидно, если кислота, например азотная
НNO 3 , диссоциирует, предположим, на два иона
и при электролизе водного раствора на катоде
(отрицательно заряженный электрод) выделяется
водород, то, следовательно, в растворе имеются
положительно заряженные ионы водорода Н + .
Тогда уравнение диссоциации следует записать
так:
НNO 3 = Н + + .
Электролитическая диссоциация
–
полный или частичный распад соединения при его
растворении в воде на ионы в результате
взаимодействия с молекулой воды (или другого
растворителя).
Электролиты
– кислоты, основания или
соли, водные растворы которых проводят
электрический ток в результате диссоциации.
Вещества, не диссоциирующие в водном растворе на
ионы и растворы которых не проводят
электрический ток, называются неэлектролитами
.
Диссоциация электролитов количественно
характеризуется степенью диссоциации
– отношением числа распавшихся на ионы
«молекул» (формульных единиц) к общему числу
«молекул» растворенного вещества. Степень
диссоциации обозначается греческой буквой . Например, если из
каждых 100 «молекул» растворенного вещества 80
распадаются на ионы, то степень диссоциации
растворенного вещества равна: = 80/100 = 0,8, или 80%.
По способности к диссоциации (или, как говорят,
«по силе») электролиты разделяют на сильные
,
средние
и слабые
. По степени
диссоциации к сильным электролитам относят те из
них, для растворов которых > 30%, к слабым – < 3%, к средним – 3% 30%. Сила электролита –
величина, зависящая от концентрации вещества,
температуры, природы растворителя и др.
В случае водных растворов
к сильным электролитам
( > 30%) относят
перечисленные ниже группы соединений.
1
. Многие неорганические кислоты,
например хлороводородная НCl, азотная HNO 3 ,
серная H 2 SО 4 в разбавленных растворах.
Самая сильная неорганическая кислота – хлорная
НСlО 4 .
Сила некислородных кислот возрастает в ряду
однотипных соединений при переходе вниз по
подгруппе кислотообразующих элементов:
HCl – HBr – HI.
Фтороводородная (плавиковая) кислота HF растворяет стекло, но это вовсе не говорит о ее силе. Эта кислота из бескислородных галогенсодержащих относится к кислотам средней силы из-за высокой энергии связи Н–F, способности молекул HF к объединению (ассоциации) благодаря сильным водородным связям, взаимодействия ионов F – с молекулами НF (водородные связи) с образованием ионов и других более сложных частиц. В результате концентрация ионов водорода в водном растворе этой кислоты оказывается значительно пониженной, поэтому фтороводородную кислоту считают средней силы.
Фтороводород реагирует с диоксидом кремния, входящим в состав стекла, по уравнению:SiO 2 + 4HF = SiF 4 + 2H 2 O.
Фтороводородную кислоту нельзя хранить в стеклянных сосудах. Для этого используют сосуды из свинца, некоторых пластмасс и стекла, стенки которых покрыты изнутри толстым слоем парафина. Если для «травления» стекла использовать газообразный фтороводород, то поверхность стекла становится матовой, что используется для нанесения на стекло надписей и различных рисунков. «Травление» стекла водным раствором фтороводородной кислоты приводит к разъеданию поверхности стекла, которая остается прозрачной. В продаже обычно бывает 40%-й раствор плавиковой кислоты.
Сила однотипных кислородных кислот изменяется
в противоположном направлении, например йодная
кислота НIО 4 слабее хлорной кислоты НСlО 4 .
Если элемент образует несколько кислородных
кислот, то наибольшей силой обладает кислота, в
которой кислотообразующий элемент имеет самую
высокую валентность. Так, в ряду кислот НСlО
(хлорноватистая) – НСlО 2 (хлористая) – НСlО 3
(хлорноватая) – НСlО 4 (хлорная) последняя
наиболее сильная.
Один объем воды растворяет около двух объемов хлора. Хлор (примерно половина его) взаимодействует с водой:
Cl 2 + H 2 O = HCl + HСlO.
Хлороводородная кислота является сильной, в ее водном растворе практически нет молекул HCl. Правильнее уравнение реакции записать так:
Cl 2 + H 2 O = H + + Cl – + HClO – 25 кДж/моль.
Образующийся раствор называют хлорной водой.
Хлорноватистая кислота – быстродействующий окислитель, поэтому ее применяют для отбеливания тканей.
2 . Гидроксиды элементов главных подгрупп I и II групп периодической системы: LiОН, NaОН, КОН, Са(ОН) 2 и др. При переходе вниз по подгруппе по мере усиления металлических свойств элемента сила гидроксидов возрастает. Растворимые гидроксиды главной подгруппы I группы элементов относят к щелочам.
Щелочами называют растворимые в воде основания. К ним относят также гидроксиды элементов главной подгруппы II группы (щелочно-земельные металлы) и гидроксид аммония (водный раствор аммиака). Иногда щелочами считают те гидроксиды, которые в водном растворе создают высокую концентрацию гидроксид-ионов. В устаревшей литературе вы можете встретить в числе щелочей карбонаты калия К 2 СО 3 (поташ) и натрия Na 2 CO 3 (сода), гидрокарбонат натрия NaHCO 3 (питьевая сода), буру Na 2 B 4 O 7 , гидросульфиды натрия NaHS и калия KHS и др.
Гидроксид кальция Са(ОН) 2 как сильный электролит диссоциирует в одну ступень:
Са(ОН) 2 = Са 2+ + 2ОН – .
3 . Почти все соли. Соль, если это сильный электролит, диссоциирует в одну ступень, например хлорид железа:
FeCl 3 = Fe 3+ + 3Cl – .
В случае водных растворов к слабым электролитам ( < 3%) относят перечисленные ниже соединения.
1 . Вода H 2 O – важнейший электролит.
2
. Некоторые неорганические и почти
все органические кислоты: H 2 S
(сероводородная), H 2 SO 3 (сернистая), H 2 CO 3
(угольная), HCN (циановодородная), Н 3 РО 4
(фосфорная, ортофосфорная), H 2 SiO 3
(кремниевая), H 3 BO 3 (борная, ортоборная),
СН 3 СООН (уксусная) и др.
Заметим, что угольная кислота в формуле H 2 CO 3
не существует. При растворении углекислого газа
СО 2 в воде образуется его гидрат СО 2 Н 2 О,
который мы для удобства расчетов записываем
формулой H 2 CO 3 , и уравнение реакции
диссоциации выглядит так:
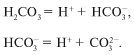
Диссоциация слабой угольной кислоты проходит в
две ступени. Образующийся гидрокарбонат-ион также ведет себя
как слабый электролит.
Точно так же ступенчато диссоциируют и другие
многоосновные кислоты: Н 3 РО 4
(фосфорная), H 2 SiO 3 (кремниевая), H 3 BO 3
(борная). В водном растворе диссоциация
практически проходит лишь по первой ступени. Как
осуществить диссоциацию по последней ступени?
3
. Гидроксиды многих элементов, например
Аl(OH) 3 , Cu(OH) 2 , Fe(OH) 2 , Fe(OH) 3 и др.
Все эти гидроксиды диссоциируют в водном
растворе ступенчато, например гидроксид железа
Fe(OH) 3:
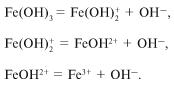
В водном растворе диссоциация проходит
практически только по первой ступени. Как
сместить равновесие в сторону образования ионов
Fe 3+ ?
Осно"вные свойства гидроксидов одного и того же
элемента усиливаются с уменьшением валентности
элемента. Так, осно"вные свойства дигидроксида
железа Fe(OH) 2 выражены сильнее, чем у
тригидроксида Fe(OH) 3 . Это утверждение
равносильно тому, что кислотные свойства Fe(OH) 3
проявляются сильнее, чем у Fe(OH) 2 .
4
. Гидроксид аммония NH 4 OH.
При растворении газообразного аммиака NH 3 в
воде получается раствор, который очень слабо
проводит электрический ток и имеет
горько-мыльный вкус. Среда раствора осно"вная,
или щелочная. Объясняется такое поведение
аммиака следующим образом. При растворении
аммиака в воде образуется гидрат аммиака NH 3 Н 2 О,
которому условно мы приписываем формулу
несуществующего гидроксида аммония NH 4 OH,
считая, что это соединение диссоциирует с
образованием иона аммония и гидроксид-иона ОН – :
NH 4 OH = + ОН – .
5 . Некоторые соли: хлорид цинка ZnCl 2 , тиоцианат железа Fe(NСS) 3 , цианид ртути Hg(CN) 2 и др. Эти соли диссоциируют ступенчато.
К электролитам средней силы некоторые относят фосфорную кислоту Н 3 РО 4 . Мы будем считать фосфорную кислоту слабым электролитом и записывать три ступени ее диссоциации. Серная кислота в концентрированных растворах ведет себя как электролит средней силы, а в очень концентрированных растворах – как слабый электролит. Мы далее будем считать серную кислоту сильным электролитом и записывать уравнение ее диссоциации в одну ступень.
Инструкция
Суть данной теории заключается в том, что при расплавлении (растворении в воде) практически все электролиты раскладываются на ионы, которые как положительно, так и отрицательно заряженные (что и называется электролитической диссоциацией). Под воздействием электрического тока отрицательные ( «-») к аноду (+), а положительно заряженные (катионы, «+»), движутся к катоду (-). Электролитическая диссоциация – это обратимый процесс (обратный процесс носит название «моляризация»).
Степень (a) электролитической диссоциации находится в зависимости от самого электролита, растворителя, и от их концентрации. Это отношение числа молекул (n) , которые распались на ионы к общему числу введенных в раствор молекул (N). Получаете: a = n / N
Таким образом, сильные электролиты - вещества, полностью распадающиеся на ионы при растворении в воде. К сильным электролитам, как правило, вещества с сильнополярными или связями: это соли, которые хорошо растворимы, (HCl, HI, HBr, HClO4, HNO3, H2SO4), а также сильные основания (KOH, NaOH, RbOH, Ba(OH)2, CsOH, Sr(OH)2, LiOH, Ca(OH)2). В сильном электролите вещество, растворенное в нем, находится по большей части в виде ионов ( ); молекул, которые недиссоциированные - практически нет.
Слабые электролиты - такие вещества, которые диссоциируют на ионы лишь частично. Слабые электролиты вместе с ионами в растворе содержат молекулы недиссоциированные. Слабые электролиты не дают в растворе сильной концентрации ионов.
К слабым относятся:
- органические кислоты (почти все) (C2H5COOH, CH3COOH и пр.);
- некоторые из кислот (H2S, H2CO3 и пр.);
- практически все соли, малорастворимые в воде, гидроксид аммония, а также все основания (Ca3(PO4)2; Cu(OH)2; Al(OH)3; NH4OH);
- вода.
Они практически не проводят электрический ток, или проводят, но плохо.
Обратите внимание
Хотя чистая вода проводит электрический ток очень плохо, она все-таки имеет измеримую электрическую проводимость, объясняемую тем, что вода немного диссоциирует на гидроксид-ионы и ионы водорода.
Полезный совет
Большинство электролитов – вещества агрессивные, поэтому при работе с ними будьте предельно осторожны и соблюдайте правила техники безопасности.
Сильное основание - неорганическое химическое соединение, образованное гидроксильной группой -ОН и щелочным (элементы I группы периодической системы: Li, K, Na, RB, Cs) или щелочноземельным металлом (элементы II группы Ba, Ca). Записываются в виде формул LiOH, KOH, NaOH, RbOH, CsOH, Са(ОН) ₂, Ва(ОН) ₂.
Вам понадобится
- выпарительная чашка
- горелка
- индикаторы
- металлический стержень
- Н₃РО₄
Инструкция
Сильные основания проявляют , характерные для всех . Наличие в растворе определяется по изменению окраски индикатора. К пробе с исследуемым раствором добавьте , фенолфталеин или опустите лакмусовую бумажку. Метилоранж дает желтую окраску, фенолфталеин – пурпурную, а лакмусовая бумага окрашивается в синий цвет. Чем сильнее основание, тем интенсивнее окрашивается индикатор.
Если необходимо узнать какие именно щелочи вам представлены, то проведите качественный анализ растворов. Наиболее распространенные сильные основания – лития, калия, натрия, бария и кальция. Основания вступают в реакцию с кислотами (реакции нейтрализации) с образованием соли и воды. При этом можно выделить Са(ОН) ₂, Ва(ОН) ₂ и LiOH. При с кислотой образуются нерастворимые . Остальные гидроксиды осадков не дадут, т.к. все соли К и Na растворимы.
3 Са(ОН) ₂ + 2 Н₃РО₄ --→ Ca₃(PO₄)₂↓+ 6 H₂О
3 Ва(ОН) ₂ +2 Н₃РО₄ --→ Ва₃(PO₄)₂↓+ 6 H₂О
3 LiOH + Н₃РО₄ --→ Li₃РО₄↓ + 3 H₂О
Процедите их и высушите. Внесите высушенные осадки в пламя горелки. По изменению окраски пламени можно качественно определить ионы лития, кальция и бария. Соответственно вы определите где какой гидроксид. Соли лития окрашивают пламя горелки в карминово-красный цвет. Соли бария – в зеленый, а соли кальция – в малиновый.
Оставшиеся щелочи образуют растворимые ортофосфаты.
3 NaOH + Н₃РО₄--→ Na₃РО₄ + 3 H₂О
3 KOH + Н₃РО₄--→ K₃РО₄ + 3 H₂О
Необходимо выпарить воду до сухого остатка. Выпаренные соли на металлическом стержне поочередно внесите в пламя горелки. Там, соль натрия – пламя окрасится в ярко-желтый цвет, а калия – в розово-фиолетовый. Таким образом имея минимальный набор оборудования и реактивов вы определили все данные вам сильные основания.
Электролит – вещество, которое в твердом состоянии является диэлектриком, то есть не проводит электрического тока, однако, в растворенном или расплавленном виде становится проводником. Почему происходит такая резкая смена свойств? Дело в том, что молекулы электролита в растворах или расплавах диссоциируют на положительно заряженные и отрицательно заряженные ионы, благодаря чему эти вещества в таком агрегатном состоянии способны проводить электрический ток. Электролитическими свойствами обладает большинство солей, кислот, оснований.

Инструкция
Какие вещества относятся к сильным ? Такие вещества, в растворах или расплавах которых подвергаются практически 100% молекул, причем вне зависимости от концентрации раствора. В перечень входит абсолютное большинство растворимых щелочей, солей и некоторые кислоты, такие как соляная, бромистая, йодистая, азотная и т.д.
А как ведут себя в растворах или расплавах слабые электролиты ? Во-первых, они диссоциируют в очень малой степени (не больше 3% от общего количества молекул), во-вторых, их идет тем хуже и медленнее, чем выше концентрация раствора. К таким электролитам относятся, например, (гидроксид аммония), большинство органических и неорганических кислот (включая плавиковую – HF) и, разумеется, всем нам знакомая вода. Поскольку лишь ничтожно малая доля ее молекул распадается на водород-ионы и гидроксил-ионы.
Запомните, что степень диссоциации и, соответственно, сила электролита находятся в зависимости факторов: природы самого электролита, растворителя, температуры. Поэтому само это разделение в известной степени условно. Ведь одно и то же вещество может при различных условиях быть и сильным электролитом, и слабым. Для оценки силы электролита была введена специальная величина – константа диссоциации, определяемая на основе закона действующих масс. Но она применима лишь по отношению к слабым электролитам; сильные электролиты закону действующих масс не подчиняются.
Источники:
- сильные электролиты список
Соли – это химические вещества, состоящие из катиона, то есть положительно заряженного иона, металла и отрицательно заряженного аниона – кислотного остатка. Типов солей много: нормальные, кислые, основные, двойные, смешанные, гидратные, комплексные. Это зависит от составов катиона и аниона. Как можно определить основание соли?

Электролиты классифицируются на две группы в зависимости от степени диссоциации - сильные и слабые электролиты. Сильные электролиты имеют степень диссоциации больше единицы или больше 30 %, слабые - меньше единицы или меньше 3 %.
Процесс диссоциация
Электролитическая диссоциация - процесс распада молекул на ионы - положительно заряженные катионы и отрицательно заряженные анионы. Заряженные частицы переносят электрический ток. Электролитическая диссоциация возможна только в растворах и расплавах.
Движущей силой диссоциации является распад ковалентных полярных связей под действием молекул воды. Полярные молекулы оттягиваются водными молекулами. В твёрдых веществах разрушаются ионные связи в процессе нагревания. Высокие температуры вызывают колебания ионов в узлах кристаллической решётки.

Рис. 1. Процесс диссоциации.
Вещества, которые легко распадаются на ионы в растворах или в расплавах и, следовательно, проводят электрический ток, называются электролитами. Неэлектролиты не проводят электричество, т.к. не распадаются на катионы и анионы.
В зависимости от степени диссоциации различают сильные и слабые электролиты. Сильные растворяются в воде, т.е. полностью, без возможности восстановления распадаются на ионы. Слабые электролиты распадаются на катионы и анионы частично. Степень их диссоциации меньше, чем у сильных электролитов.
Степень диссоциация показывает долю распавшихся молекул в общей концентрации веществ. Она выражается формулой α = n/N.

Рис. 2. Степень диссоциации.
Слабые электролиты
Список слабых электролитов:
- разбавленные и слабые неорганические кислоты - H 2 S, H 2 SO 3 , H 2 CO 3 , H 2 SiO 3 , H 3 BO 3 ;
- некоторые органические кислоты (большинство органических кислот - неэлектролиты) - CH 3 COOH, C 2 H 5 COOH;
- нерастворимые основания - Al(OH) 3 , Cu(OH) 2 , Fe(OH) 2 , Zn(OH) 2 ;
- гидроксид аммония - NH 4 OH.

Рис. 3. Таблица растворимости.
Реакция диссоциации записывается с помощью ионного уравнения:
- HNO 2 ↔ H + + NO 2 – ;
- H 2 S ↔ H + + HS – ;
- NH 4 OH ↔ NH 4 + + OH – .
Многоосновные кислоты диссоциируют ступенчато:
- H 2 CO 3 ↔ H + + HCO 3 – ;
- HCO 3 – ↔ H + + CO 3 2- .
Нерастворимые основания также распадаются поэтапно:
- Fe(OH) 3 ↔ Fe(OH) 2 + + OH – ;
- Fe(OH) 2 + ↔ FeOH 2+ + OH – ;
- FeOH 2+ ↔ Fe 3+ + OH – .
Воду относят к слабым электролитам. Вода практически не проводит электрический ток, т.к. слабо распадается на катионы водорода и анионы гироксид-иона. Образовавшиеся ионы обратно собираются в молекулы воды:
H 2 O ↔ H + + OH – .
Если вода легко проводит электричество, значит, в ней есть примеси. Дистиллированная вода неэлектропроводная.
Диссоциация слабых электролитов обратима. Образовавшиеся ионы вновь собираются в молекулы.
Что мы узнали?
К слабым электролитам относятся вещества, частично распадающиеся на ионы - положительные катионы и отрицательные анионы. Поэтому такие вещества плохо проводят электрический ток. К ним относятся слабые и разбавленные кислоты, нерастворимые основания, малорастворимые соли. Наиболее слабый электролит - вода. Диссоциация слабых электролитов - обратимая реакция.
Электролиты как химические вещества известны с древних времён. Однако большинство областей своего применения они завоевали относительно недавно. Мы обсудим самые приоритетные для промышленности области использования этих веществ и разберёмся, что же последние собой представляют и чем отличаются друг от друга. Но начнём с экскурса в историю.
История
Самые старые известные электролиты - это соли и кислоты, открытые ещё в Древнем мире. Однако представления о строении и свойствах электролитов развивались со временем. Теории этих процессов эволюционировали, начиная с 1880 годов, когда был сделан ряд открытий, связанный с теориями свойств электролитов. Наблюдались несколько качественных скачков в теориях, описывающих механизмы взаимодействия электролитов с водой (ведь только в растворе они приобретают те свойства, благодаря которым их используют в промышленности).
Сейчас мы подробно разберём несколько теорий, оказавших наибольшее влияние на развитие представлений об электролитах и их свойствах. И начнём с самой распространённой и простой теории, которую каждый из нас проходил в школе.
Теория электролитической диссоциации Аррениуса
в 1887 году шведский химик и Вильгельм Оствальд создали теорию электролитической диссоциации. Однако тут тоже не всё так просто. Сам Аррениус был сторонником так называемой физической теории растворов, которая не учитывала взаимодействие составляющих вещества с водой и утверждала, что в растворе существуют свободные заряженные частицы (ионы). Кстати, именно с таких позиций сегодня рассматривают электролитическую диссоциацию в школе.
Поговорим всё-таки о том, что даёт эта теория и как она объясняет нам механизм взаимодействия веществ с водой. Как и у любой другой, у неё есть несколько постулатов, которые она использует:
1. При взаимодействии с водой вещество распадается на ионы (положительный - катион и отрицательный - анион). Эти частицы подвергаются гидратации: они притягивают молекулы воды, которые, кстати, заряжены с одной стороны положительно, а с другой - отрицательно (образуют диполь), в результате формируются в аквакомплексы (сольваты).
2. Процесс диссоциации обратим - то есть если вещество распалось на ионы, то под действием каких-либо факторов оно вновь может превратиться в исходное.
3. Если подключить к раствору электроды и пустить ток, то катионы начнут движение к отрицательному электроду - катоду, а анионы к положительно заряженному - аноду. Именно поэтому вещества, хорошо растворимые в воде, проводят электрический ток лучше, чем сама вода. По той же причине их назвали электролитами.
4. электролита характеризует процент вещества, подвергшегося растворению. Этот показатель зависит от свойств растворителя и самого растворённого вещества, от концентрации последнего и от внешней температуры.
Вот, по сути, и все основные постулаты этой несложной теории. Ими мы будем пользоваться в этой статье для описания того, что же происходит в растворе электролита. Примеры этих соединений разберём чуть позже, а сейчас рассмотрим другую теорию.

Теория кислот и оснований Льюиса
По теории электролитической диссоциации, кислота - это вещество, в растворе которого присутствует катион водорода, а основание - соединение, распадающееся в растворе на гидроксид-анион. Существует другая теория, названная именем известного химика Гилберта Льюиса. Она позволяет несколько расширить понятие кислоты и основания. По теории Льюиса, кислоты - или молекулы вещества, которые имеют свободные электронные орбитали и способны принять электрон от другой молекулы. Несложно догадаться, что основаниями будут являться такие частицы, которые способны отдать один или несколько своих электронов в "пользование" кислоте. Очень интересно здесь то, что кислотой или основанием может быть не только электролит, но и любое вещество, даже нерастворимое в воде.

Протолитическая теория Брендстеда-Лоури
В 1923 году, независимо друг от друга, двое учёных - Й. Бренстед и Т. Лоури -предложили теорию, которая сейчас активно применяется учёными для описания химических процессов. Суть этой теории в том, что смысл диссоциации сводится к передаче протона от кислоты основанию. Таким образом, последнее понимается здесь как акцептор протонов. Тогда кислота является их донором. Теория также хорошо объясняет существование веществ, проявляющих свойства и кислоты и основания. Такие соединения называются амфотерными. В теории Бренстеда-Лоури для них также применяется термин амфолиты, тогда как кислота или основания принято называть протолитами.
Мы подошли к следующей части статьи. Здесь мы расскажем, чем отличаются друг от друга сильные и слабые электролиты и обсудим влияние внешних факторов на их свойства. А затем уже приступим к описанию их практического применения.
Сильные и слабые электролиты
Каждое вещество взаимодействует с водой индивидуально. Какие-то растворяются в ней хорошо (например, поваренная соль), а какие-то совсем не растворяются (например, мел). Таким образом, все вещества делятся на сильные и слабые электролиты. Последние представляют собой вещества, плохо взаимодействующие с водой и оседающие на дне раствора. Это означает, что они имеют очень низкую степень диссоциации и высокую энергию связей, которая не позволяет при нормальных условиях распадаться молекуле на составляющие её ионы. Диссоциация слабых электролитов происходит либо очень медленно, либо при повышении температуры и концентрации этого вещества в растворе.
Поговорим о сильных электролитах. К ним можно отнести все растворимые соли, а также сильные кислоты и щёлочи. Они легко распадаются на ионы и очень трудно собрать их в осадки. Ток в электролитах, кстати, проводится именно благодаря ионам, содержащимся в растворе. Поэтому лучше всех проводят ток сильные электролиты. Примеры последних: сильные кислоты, щёлочи, растворимые соли.

Факторы, влияющие на поведение электролитов
Теперь разберёмся, как влияет изменение внешней обстановки на Концентрация напрямую влияет на степень диссоциации электролита. Более того, это соотношение можно выразить математически. Закон, описывающий эту связь, называется законом разбавления Оствальда и записывается так: a = (K / c) 1/2 . Здесь a - это степень диссоциации (берётся в долях), К - константа диссоциации, разная для каждого вещества, а с - концентрация электролита в растворе. По этой формуле можно узнать много нового о веществе и его поведении в растворе.
Но мы отклонились от темы. Кроме концентрации, на степень диссоциации также влияет температура электролита. Для большинства веществ её увеличение повышает растворимость и химическую активность. Именно этим можно объяснить протекание некоторых реакций только при повышенной температуре. При нормальных условиях они идут либо очень медленно, либо в обе стороны (такой процесс называется обратимым).
Мы разобрали факторы, определяющие поведение такой системы, как раствор электролита. Сейчас перейдём к практическому применению этих, без сомнения, очень важных химических веществ.

Промышленное использование
Конечно, все слышали слово "электролит" применительно к аккумуляторам. В автомобиле используют свинцово-кислотные аккумуляторы, роль электролита в котором выполняет 40-процентная серная кислота. Чтобы понять, зачем там вообще нужно это вещество, стоит разобраться в особенностях работы аккумуляторов.
Так в чём принцип работы любого аккумулятора? В них происходит обратимая реакция превращения одного вещества в другое, в результате которой высвобождаются электроны. При заряде аккумулятора происходит взаимодействие веществ, которого не получается при нормальных условиях. Это можно представить как накопление электроэнергии в веществе в результате химической реакции. При разряде же начинается обратное превращение, приводящее систему к начальному состоянию. Эти два процесса вместе составляют один цикл заряда-разряда.
Рассмотрим вышеизложенный процесс на конкретном примере - свинцово-кислотном аккумуляторе. Как нетрудно догадаться, этот источник тока состоит из элемента, содержащего свинец (а также диокисд свинца PbO 2) и кислоты. Любой аккумулятор состоит из электродов и пространства между ними, заполненного как раз электролитом. В качестве последнего, как мы уже выяснили, в нашем примере используется серная кислота концентрацией 40 процентов. Катод такого аккумулятора делают из диоксида свинца, а анод состоит из чистого свинца. Всё это потому, что на этих двух электродах протекают разные обратимые реакции с участием ионов, на которые продиссоциировала кислота:
- PbO 2 + SO 4 2- + 4H + + 2e - = PbSO 4 + 2H 2 O (реакция, происходящая на отрицательном электроде - катоде).
- Pb + SO 4 2- - 2e - = PbSO 4 (Реакция, протекающая на положительном электроде - аноде).
Если читать реакции слева направо - получаем процессы, происходящие при разряде аккумулятора, а если справа налево - при заряде. В каждом эти реакции разные, но механизм их протекания в общем описывается одинаково: происходят два процесса, в одном из которых электроны "поглощаются", а в другом, наоборот, "выходят". Самое главное то, что число поглощённых электронов равно числу вышедших.
Собственно, кроме аккумуляторов, существует масса применений этих веществ. Вообще, электролиты, примеры которых мы привели, - это лишь крупинка того многообразия веществ, которые объединены под этим термином. Они окружают нас везде, повсюду. Вот, например, тело человека. Думаете, там нет этих веществ? Очень ошибаетесь. Они находятся везде в нас, а самое большое количество составляют электролиты крови. К ним относятся, например, ионы железа, которые входят в состав гемоглобина и помогают транспортировать кислород к тканям нашего организма. Электролиты крови также играют ключевую роль в регуляции водно-солевого баланса и работе сердца. Эту функцию выполняют ионы калия и натрия (существует даже процесс, происходящий в клетках, который назвается калий-натриевым насосом).
Любые вещества, которые вы в силах растворить хоть немного, - электролиты. И нет такой отрасли промышленности и нашей с вами жизни, где бы они ни применялись. Это не только аккумуляторы в автомобилях и батарейки. Это любое химическое и пищевое производство, военные заводы, швейные фабрики и так далее.
Состав электролита, кстати, бывает разным. Так, можно выделить кислотный и щелочной электролит. Они принципиально отличаются своими свойствами: как мы уже говорили, кислоты являются донорами протонов, а щёлочи - акцепторами. Но со времением состав электролита меняется вследствие потери части вещества концентрация либо уменьшается, либо увеличивается (всё зависит от того, что теряется, вода или электролит).
Мы каждый день сталкиваемся с ними, однако мало кто точно знает определение такого термина, как электролиты. Примеры конкретных веществ мы разобрали, поэтому перейдём к немного более сложным понятиям.

Физические свойства электролитов
Теперь о физике. Самое важное, что нужно понимать при изучении этой темы - как передаётся ток в электролитах. Определяющую роль в этом играют ионы. Эти заряженные частицы могут переносить заряд из одной части раствора в другую. Так, анионы стремятся всегда к положительному электроду, а катионы - к отрицательному. Таким образом, действуя на раствор электрическим током, мы разделяем заряды по разным сторонам системы.
Очень интересна такая физическая характеристика, как плотность. От неё зависят многие свойства обсуждаемых нами соединений. И зачастую всплывает вопрос: "Как поднять плотность электролита?" На самом деле ответ прост: необходимо понизить содержание воды в растворе. Так как плотность электролита большей частью определяется то она большей частью зависит от концентрации последней. Существует два способа осуществить задуманное. Первый достаточно простой: прокипятить электролит, содержащийся в аккумуляторе. Для этого нужно зарядить его так, чтобы температура внутри поднялась чуть выше ста градусов по цельсию. Если этот способ не помогает, не переживайте, существует ещё один: просто-напросто заменить старый электролит новым. Для этого нужно слить старый раствор, прочистить внутренности от остатков серной кислоты дистиллированной водой, а затем залить новую порцию. Как правило, качественные растворы электролита сразу имеют нужную величину концентрации. После замены можете надолго забыть о том, как поднять плотность электролита.
Состав электролита во многом определяет его свойства. Такие характеристики, как электропроводность и плотность, например, сильно зависят от природы растворённого вещества и его концентрации. Существует отдельный вопрос о том, сколько электролита в аккумуляторе может быть. На самом деле его объём напрямую связан с заявленной мощностью изделия. Чем больше серной кислоты внутри аккумулятора, тем он мощнее, т. е. тем большее напряжение способен выдавать.

Где это пригодится?
Если вы автолюбитель или просто увлекаетесь автомобилями, то вы и сами всё понимаете. Наверняка вы даже знаете, как определить, сколько электролита в аккумуляторе находится сейчас. А если вы далеки от автомобилей, то знание свойств этих веществ, их применения и того, как они взаимодействуют друг с другом будет совсем не лишним. Зная это, вы не растеряетесь, если вас попросят сказать, какой электролит в аккумуляторе. Хотя даже если вы не автолюбитель, но у вас есть машина, то знание устройства аккумулятора будет совсем не лишним и поможет вам в ремонте. Будет гораздо легче и дешевле сделать всё самому, нежели ехать в автоцентр.
А чтобы лучше изучить эту тему, мы рекомендуем почитать учебник химии для школы и вузов. Если вы хорошо знаете эту науку и прочитали достаточно учебников, лучшим вариантом будут "Химические источники тока" Варыпаева. Там изложены подробно вся теория работы аккумуляторов, различных батарей и водородных элементов.
Заключение
Мы подошли к концу. Подведём итоги. Выше мы разобрали всё, что касается такого понятия, как электролиты: примеры, теория строения и свойств, функции и применение. Ещё раз стоит сказать, что эти соединения составляют часть нашей жизни, без которой не могли бы существовать наши тела и все сферы промышленности. Вы помните про электролиты крови? Благодаря им мы живём. А что насчёт наших машин? С помощью этих знаний мы сможем исправить любую проблему, связанную с аккумулятором, так как теперь понимаем, как поднять плотность электролита в нём.
Всё рассказать невозможно, да мы и не ставили такой цели. Ведь это далеко не всё, что можно рассказать об этих удивительных веществах.