Слабые электролиты примеры. Электролиты: примеры. Состав и свойства электролитов. Сильные и слабые электролиты
Сильные и слабые электролиты
Кислоты, основания и соли в водных растворах диссоциируют — распадаются на ионы. Этот процесс может быть обратимым или необратимым.
При необратимой диссоциации в растворах все вещество или почти все распадается на ионы. Это характерно для сильных электролитов (рис. 10.1, а, с. 56). К сильным электролитам относятся некоторые кислоты и все растворимые в воде соли и основания (гидроксиды щелочных и щелочноземельных элементов) (схема 5, с. 56).
Рис. 10.1. Сравнение числа ионов в растворах с одинаковым исходным количеством электролита: а — хлоридная кислота (сильный электролит); б — нитритная кислота
(слабый электролит)
Схема 5. Классификация электролитов по силе

При обратимой диссоциации протекает два противоположных процесса: одновременно с распадом вещества на ионы (диссоциацией) происходит обратный процесс объединения ионов в молекулы вещества (ассоциация). Благодаря этому часть вещества в растворе существует в виде ионов, а часть — в виде молекул (рис. 10.1, б). Электролиты,
которые при растворении в воде распадаются на ионы только частично, называют слабыми электролитами. К их числу относится вода, многие кислоты, а также нерастворимые гидроксиды и соли (схема 5).
В уравнениях диссоциации слабых электролитов вместо обычной стрелки записывают двунаправленную стрелку (знак обратимости):
![]()
Силу электролитов можно объяснить полярностью химической связи, которая разрывается при диссоциации. Чем более полярна связь, тем легче под действием молекул воды она превращается в ионную, следовательно, тем сильнее электролит. В солях и гидроксидах полярность связи наибольшая, поскольку между ионами металлических элементов, кислотными остатками и гидроксид-ионами существует ионная связь, поэтому все растворимые соли и основания — сильные электролиты. В оксигенсодержащих кислотах при диссоциации разрывается связь O-H, полярность которой зависит от качественного и количественного состава кислотного остатка. Силу большинства оксигенсодержащих кислот можно определить, если обычную формулу кислоты записать в виде E(OH) m O n . Если в этой формуле будет n < 2 — кислота слабая, если n >2 — сильная.
Зависимость силы кислот от состава кислотного остатка

Степень диссоциации
Силу электролитов количественно характеризует степень электролитической диссоциации а, показывающая долю молекул вещества, которые распались в растворе на ионы.
Степень диссоциации а равна отношению числа молекул N или количества вещества n, распавшегося на ионы, к общему числу молекул N 0 или количеству растворенного вещества n 0:
Степень диссоциации можно выражать не только в долях единицы, но и в процентах:
Значение а может изменяться от 0 (диссоциация отсутствует) до 1, или 100 % (полная диссоциация). Чем лучше распадается электролит, тем больше значение степени диссоциации.
По значению степени электролитической диссоциации электролиты часто разделяют не на две, а на три группы: сильные, слабые и электролиты средней силы. Сильными электролитами считают те, степень диссоциации которых более 30 %, а слабыми — со степенью менее 3 %. Электролиты с промежуточными значениями а — от 3 % до 30 % — называют электролитами средней силы. По этой классификации таковыми считаются кислоты: HF, HNO 2 , H 3 PO 4 , H 2 SO 3 и некоторые другие. Две последние кислоты являются электролитами средней силы только по первой стадии диссоциации, а по другим — это слабые электролиты.
Степень диссоциации — величина переменная. Она зависит не только от природы электролита, но и от его концентрации в растворе. Эту зависимость впервые определил и исследовал Вильгельм Оствальд. Сегодня ее называют законом разведения Оствальда: при разбавлении раствора водой, а также при повышении температуры степень диссоциации увеличивается.
Вычисление степени диссоциации
Пример. В одном литре воды растворили гидроген флуорид количеством вещества 5 моль. Полученный раствор содержит 0,06 моль ионов Гидрогена. Определите степень диссоциации флуоридной кислоты (в процентах).

Запишем уравнение диссоциации флуоридной кислоты:
При диссоциации из одной молекулы кислоты образуется один ион Гидрогена. Если в растворе содержится 0,06 моль ионов H+, это означает, что продиссоцииро-вало 0,06 моль молекул гидроген флуорида. Следовательно, степень диссоциации равна:


Выдающийся немецкий физико-химик, лауреат Нобелевской премии по химии 1909 года. Родился в Риге, учился в Дерптском университете, где начал преподавательскую и научную деятельность. В 35 лет переехал в Лейпциг, где возглавил Физико-химический институт. Изучал законы химического равновесия, свойства растворов, открыл закон разведения, названный его именем, разработал основы теории кислотно-основного катализа, много времени уделял истории химии. Основал первую в мире кафедру физической химии и первый физико-химический журнал. В личной жизни обладал странными привычками: чувствовал отвращение к стрижке, а со своим секретарем общался исключительно при помощи велосипедного звонка.
Ключевая идея
Диссоциация слабых электролитов — обратимый процесс, а сильных —
необратимый.
Контрольные вопросы
116. Дайте определение сильных и слабых электролитов.
117. Приведите примеры сильных и слабых электролитов.
118. Какую величину используют для количественной характеристики силы электролита? Является ли она постоянной в любых растворах? Как можно увеличить степень диссоциации электролита?
Задания для усвоения материала
119. Приведите по одному примеру соли, кислоты и основания, которые являются: а) сильным электролитом; б) слабым электролитом.
120. Приведите пример вещества: а) двухосновная кислота, которая по первой стадии является электролитом средней силы, а по второй — слабым электролитом; б) двухосновная кислота, которая по обеим стадиями является слабым электролитом.
121. В некоторой кислоте по первой стадии степень диссоциации составляет 100 %, а по второй — 15 %. Какая кислота это может быть?
122. Каких частиц больше в растворе гидроген сульфида: молекул H 2 S, ионов H+, ионов S 2- или ионов HS - ?
123. Из приведенного перечня веществ отдельно выпишите формулы: а) сильных электролитов; б) слабых электролитов.
NaCl, HCl, NaOH, NaNO 3 , HNO 3 , HNO 2 , H 2 SO 4 , Ba(OH) 2 , H 2 S, K 2 S, Pb(NO 3) 2 .
124. Составьте уравнения диссоциации стронций нитрата, меркурий(11) хлорида, кальций карбоната, кальций гидроксида, сульфидной кислоты. В каких случаях диссоциация происходит обратимо?
125. В водном растворе натрий сульфата содержится 0,3 моль ионов. Какую массу этой соли использовали для приготовления такого раствора?
126. В растворе гидроген флуорида объемом 1 л содержится 2 г этой кислоты, а количество вещества ионов Гидрогена составляет 0,008 моль. Какое количество вещества флуорид-ионов в этом растворе?
127. В трех пробирках содержатся одинаковые объемы растворов хлорид-ной, флуоридной и сульфидной кислот. Во всех пробирках количества вещества кислот равны. Но в первой пробирке количество вещества ионов Гидрогена составляет 3 . 10 -7 моль, во второй — 8 . 10 -5 моль, а в третьей — 0,001 моль. В какой пробирке содержится каждая кислота?
128. В первой пробирке содержится раствор электролита, степень диссоциации которого составляет 89 %, во второй — электролит со степенью диссоциации 8 %о, а в третьей — 0,2 %о. Приведите по два примера электролитов разных классов соединений, которые могут содержаться в этих пробирках.
129*. В дополнительных источниках найдите информацию о зависимости силы электролитов от природы веществ. Установите зависимость между строением веществ, природой химических элементов, которые их образуют, и силой электролитов.
Это материал учебника
Различают сильные и слабые электролиты. Сильные электролиты в растворах практически диссоциированы полностью. К этой группе электролитов относится большинство солей, щелочей и сильных кислот. К слабым электролитам принадлежат слабые кислоты и слабые основания и некоторые соли: хлорид ртути (II), цианид ртути (II), роданид железа (III), иодид кадмия. Растворы сильных электролитов при больших концентрациях обладают значительной электропроводностью, причем она с разбавлением растворов возрастает незначительно.
Растворы слабых электролитов при больших концентрациях отличаются незначительной электропроводностью, сильно увеличивающейся при разбавлении растворов.
При растворении вещества в каком-либо растворителе образуются простые (несольватированные) ионы, нейтральные молекулы растворенного вещества, сольватированные (в водных растворах гидратированные) ионы (например, и т. д.), ионные пары (или ионные двойники), представляющие собой электростатически ассоциированные группы противоположно заряженных ионов (например, ), образование которых наблюдается в подавляющем числе неводных растворов электролитов, комплексные ионы (например, ), сольватированные молекулы и др.
В водных растворах сильных электролитов существуют только простые или сольватированные катионы и анионы. В их растворах нет молекул растворенного вещества. Поэтому неверно предполагать наличие молекул или наличие длительных связей между или и в водном растворе хлорида натрия.
В водных растворах слабых электролитов растворенное вещество может существовать в виде простых и сольватированных (-гидратированных) ионов и недиссоциированных молекул.
В неводных растворах некоторые сильные электролиты (например, ) диссоциированы не полностью даже при умеренно высоких концентрациях. В большинстве органических растворителей наблюдается образование ионных пар противоположно заряженных ионов (нодробнее см. книга 2).
В ряде случаев невозможно провести резкую границу между сильными и слабыми электролитами.
Межионные силы. Под действием межионных сил вокруг каждого свободно движущегося иона группируются, располагаясь симметрично, другие ионы, заряженные обратным знаком, образуя так называемую ионную атмосферу, или ионное облако, замедляющее движение иона в растворе.
Например, в растворе вокруг движущихся ионов калия группируются ионы хлора, а вблизи движущихся ионов хлора создается атмосфера из ионов калия.
Ионы, подвижность которых ослаблена силами межионного протяжения, проявляют в растворах пониженную химическую активность. Это вызывает отклонения в поведении сильных электролитов от классической формы закона действия масс.
Посторонние ионы, присутствующие в растворе данного электролита, также оказывают сильное влияние на подвижность его ионов. Чем выше концентрация, тем значительнее межионное взаимодействие и тем сильнее посторонние ионы влияют на подвижность ионов.
У слабых кислот и оснований связь водорода или гидроксила в их молекулах является в значительной степени не ионной, а ковалентной; поэтому при растворении слабых электролитов в растворителях, отличающихся даоюе большой диэлектрической проницаемостью, большая часть их молекул не распадается на ионы.
Растворы сильных электролитов отличаются от растворов слабых электролитов тем, что в них нет недиссоциированных молекул. Это подтверждается современными физическими и физико-химическими исследованиями. Например, исследование кристаллов сильных электролитов типа рентгенографическим путем подтверждает тот факт, что кристаллические решетки солей построены из ионов.
При растворении в растворителе с большой диэлектрической проницаемостью вокруг ионов образуются сольватные (в воде гидратные) оболочки, препятствующие их соединению в молекулы. Таким образом, поскольку сильные электролиты даже в кристаллическом состоянии не содержат молекул, они тем более не содержат молекул в растворах.
Однако экспериментальным путем найдено, что электропроводность водных растворов сильных электролитов не эквивалентна той электропроводности, которую молено было бы ожидать при -ной диссоциации молекул растворенных электролитов на ионы.
С помощью теории электролитической диссоциаций, предложенной Аррениусом, оказалось невозможным объяснить этот и ряд других фактов. Для их объяснения были выдвинуты новые научные положения.
В настоящее время несоответствие свойств сильных электролитов классической форме закона действия масс может быть объяснено при помощи теории сильных электролитов, предложенной Дебаем и Хюкке-лем. Основная идея этой теории заключается в том, что в растворах между ионами сильных электролитов возникают силы взаимного притяжения. Эти межионные силы вызывают отклонение поведения сильных электролитов от законов идеальных растворов. Наличие этих взаимодействий вызывает взаимное торможение катионов и анионов.
Влияние разбавления на межионное притяжение. Межионное притяжение вызывает отклонения в поведении реальных растворов аналогично тому, как межмолекулярное притяжение в реальных газах влечет за собой отступления их поведения от законов идеальных газов. Чем больше концентрация раствора, тем плотнее ионная атмосфера и тем меньше подвижность ионов, а следовательно, и электропроводность электролитов.
Подобно тому как свойства реального газа при низких давлениях приближаются к свойствам газа идеального, так и свойства растворов сильных электролитов при большом разбавлении приближаются к свойствам идеальных растворов.
Иными словами, в разбавленных растворах расстояния между ионами настолько велики, что испытываемое ионами взаимное притяжение или отталкивание чрезвычайно мало и практически сводится к нулю.
Таким образом, наблюдаемое увеличение электропроводности сильных электролитов при разбавлении их растворов объясняется ослаблением межионных сил притяжения и отталкивания, обусловливающим увеличение скорости движения ионов.
Чем менее диссоциирован электролит и чем более разбавлен раствор, тем меньше межионное электрическое влияние и тем меньше наблюдается отклонений от закона действия масс, и, наоборот, чем больше концентрация раствора, тем больше межионное электрическое влияние и тем больше наблюдается отклонений от закона действия масс.
По указанным выше причинам к водным растворам сильных электролитов, а также к концентрированным водным растворам слабых электролитов нельзя применять закон действия масс в его классической форме.
Инструкция
Суть данной теории заключается в том, что при расплавлении (растворении в воде) практически все электролиты раскладываются на ионы, которые как положительно, так и отрицательно заряженные (что и называется электролитической диссоциацией). Под воздействием электрического тока отрицательные ( «-») к аноду (+), а положительно заряженные (катионы, «+»), движутся к катоду (-). Электролитическая диссоциация – это обратимый процесс (обратный процесс носит название «моляризация»).
Степень (a) электролитической диссоциации находится в зависимости от самого электролита, растворителя, и от их концентрации. Это отношение числа молекул (n) , которые распались на ионы к общему числу введенных в раствор молекул (N). Получаете: a = n / N
Таким образом, сильные электролиты - вещества, полностью распадающиеся на ионы при растворении в воде. К сильным электролитам, как правило, вещества с сильнополярными или связями: это соли, которые хорошо растворимы, (HCl, HI, HBr, HClO4, HNO3, H2SO4), а также сильные основания (KOH, NaOH, RbOH, Ba(OH)2, CsOH, Sr(OH)2, LiOH, Ca(OH)2). В сильном электролите вещество, растворенное в нем, находится по большей части в виде ионов ( ); молекул, которые недиссоциированные - практически нет.
Слабые электролиты - такие вещества, которые диссоциируют на ионы лишь частично. Слабые электролиты вместе с ионами в растворе содержат молекулы недиссоциированные. Слабые электролиты не дают в растворе сильной концентрации ионов.
К слабым относятся:
- органические кислоты (почти все) (C2H5COOH, CH3COOH и пр.);
- некоторые из кислот (H2S, H2CO3 и пр.);
- практически все соли, малорастворимые в воде, гидроксид аммония, а также все основания (Ca3(PO4)2; Cu(OH)2; Al(OH)3; NH4OH);
- вода.
Они практически не проводят электрический ток, или проводят, но плохо.
Обратите внимание
Хотя чистая вода проводит электрический ток очень плохо, она все-таки имеет измеримую электрическую проводимость, объясняемую тем, что вода немного диссоциирует на гидроксид-ионы и ионы водорода.
Полезный совет
Большинство электролитов – вещества агрессивные, поэтому при работе с ними будьте предельно осторожны и соблюдайте правила техники безопасности.
Сильное основание - неорганическое химическое соединение, образованное гидроксильной группой -ОН и щелочным (элементы I группы периодической системы: Li, K, Na, RB, Cs) или щелочноземельным металлом (элементы II группы Ba, Ca). Записываются в виде формул LiOH, KOH, NaOH, RbOH, CsOH, Са(ОН) ₂, Ва(ОН) ₂.
Вам понадобится
- выпарительная чашка
- горелка
- индикаторы
- металлический стержень
- Н₃РО₄
Инструкция
Сильные основания проявляют , характерные для всех . Наличие в растворе определяется по изменению окраски индикатора. К пробе с исследуемым раствором добавьте , фенолфталеин или опустите лакмусовую бумажку. Метилоранж дает желтую окраску, фенолфталеин – пурпурную, а лакмусовая бумага окрашивается в синий цвет. Чем сильнее основание, тем интенсивнее окрашивается индикатор.
Если необходимо узнать какие именно щелочи вам представлены, то проведите качественный анализ растворов. Наиболее распространенные сильные основания – лития, калия, натрия, бария и кальция. Основания вступают в реакцию с кислотами (реакции нейтрализации) с образованием соли и воды. При этом можно выделить Са(ОН) ₂, Ва(ОН) ₂ и LiOH. При с кислотой образуются нерастворимые . Остальные гидроксиды осадков не дадут, т.к. все соли К и Na растворимы.
3 Са(ОН) ₂ + 2 Н₃РО₄ --→ Ca₃(PO₄)₂↓+ 6 H₂О
3 Ва(ОН) ₂ +2 Н₃РО₄ --→ Ва₃(PO₄)₂↓+ 6 H₂О
3 LiOH + Н₃РО₄ --→ Li₃РО₄↓ + 3 H₂О
Процедите их и высушите. Внесите высушенные осадки в пламя горелки. По изменению окраски пламени можно качественно определить ионы лития, кальция и бария. Соответственно вы определите где какой гидроксид. Соли лития окрашивают пламя горелки в карминово-красный цвет. Соли бария – в зеленый, а соли кальция – в малиновый.
Оставшиеся щелочи образуют растворимые ортофосфаты.
3 NaOH + Н₃РО₄--→ Na₃РО₄ + 3 H₂О
3 KOH + Н₃РО₄--→ K₃РО₄ + 3 H₂О
Необходимо выпарить воду до сухого остатка. Выпаренные соли на металлическом стержне поочередно внесите в пламя горелки. Там, соль натрия – пламя окрасится в ярко-желтый цвет, а калия – в розово-фиолетовый. Таким образом имея минимальный набор оборудования и реактивов вы определили все данные вам сильные основания.
Электролит – вещество, которое в твердом состоянии является диэлектриком, то есть не проводит электрического тока, однако, в растворенном или расплавленном виде становится проводником. Почему происходит такая резкая смена свойств? Дело в том, что молекулы электролита в растворах или расплавах диссоциируют на положительно заряженные и отрицательно заряженные ионы, благодаря чему эти вещества в таком агрегатном состоянии способны проводить электрический ток. Электролитическими свойствами обладает большинство солей, кислот, оснований.

Инструкция
Какие вещества относятся к сильным ? Такие вещества, в растворах или расплавах которых подвергаются практически 100% молекул, причем вне зависимости от концентрации раствора. В перечень входит абсолютное большинство растворимых щелочей, солей и некоторые кислоты, такие как соляная, бромистая, йодистая, азотная и т.д.
А как ведут себя в растворах или расплавах слабые электролиты ? Во-первых, они диссоциируют в очень малой степени (не больше 3% от общего количества молекул), во-вторых, их идет тем хуже и медленнее, чем выше концентрация раствора. К таким электролитам относятся, например, (гидроксид аммония), большинство органических и неорганических кислот (включая плавиковую – HF) и, разумеется, всем нам знакомая вода. Поскольку лишь ничтожно малая доля ее молекул распадается на водород-ионы и гидроксил-ионы.
Запомните, что степень диссоциации и, соответственно, сила электролита находятся в зависимости факторов: природы самого электролита, растворителя, температуры. Поэтому само это разделение в известной степени условно. Ведь одно и то же вещество может при различных условиях быть и сильным электролитом, и слабым. Для оценки силы электролита была введена специальная величина – константа диссоциации, определяемая на основе закона действующих масс. Но она применима лишь по отношению к слабым электролитам; сильные электролиты закону действующих масс не подчиняются.
Источники:
- сильные электролиты список
Соли – это химические вещества, состоящие из катиона, то есть положительно заряженного иона, металла и отрицательно заряженного аниона – кислотного остатка. Типов солей много: нормальные, кислые, основные, двойные, смешанные, гидратные, комплексные. Это зависит от составов катиона и аниона. Как можно определить основание соли?

Все вещества можно разделить на электролиты и неэлектролиты. К электролитам относятся вещества, растворы или расплавы которых проводят электрический ток (например, водные растворы или расплавы KCl, H 3 PO 4 , Na 2 CO 3). Вещества неэлектролиты при расплавлении или растворении электрический ток не проводят (сахар, спирт, ацетон и др.).
Электролиты подразделяются на сильные и слабые. Сильные электролиты в растворах или расплавах полностью диссоциируют на ионы. При написании уравнений химических реакций это подчеркивается стрелкой в одном направлении, например:
HCl→ H + + Cl -
Ca(OH) 2 → Ca 2+ + 2OH -
К сильным электролитам относятся вещества с гетерополярной или ионной кристаллической структурой (таблица 1.1).
Таблица 1.1 Сильные электролиты
Слабые электролиты на ионы распадаются лишь частично. Наряду с ионами в расплавах или растворах данных веществ присутствуют в подавляющем большинстве недиссоциированные молекулы. В растворах слабых электролитов параллельно с диссоциацией протекает обратный процесс - ассоциация, т.е соединение ионов в молекулы. При записи уравнения реакции это подчеркивается двумя противоположно направленными стрелками.
CH 3 COOH D CH 3 COO - + H +
К слабым электролитам относятся вещества с гомеополярным типом кристаллической решетки (таблица 1.2).
Таблица 1.2 Слабые электролиты
Равновесное состояние слабого электролита в водном растворе количественно характеризуют степенью электролитической диссоциации и константой электролитической диссоциации.
Степень электролитической диссоциации α представляет собой отношение числа молекул, распавшихся на ионы, к общему числу молекул растворенного электролита:
Степень диссоциации показывает, какая часть от общего количества растворенного электролита распадается на ионы и зависит от природы электролита и растворителя, а также от концентрации вещества в растворе, имеет безразмерную величину, хотя обыкновенно ее выражают в процентах. При бесконечном разбавлении раствора электролита степень диссоциации приближается к единице, что соответствует полной, 100%-ной, диссоциации молекул растворенного вещества на ионы. Для растворов слабых электролитов α <<1. Сильные электролиты в растворах диссоциируют полностью (α =1). Если известно, что в 0,1 М растворе уксусной кислоты степень электрической диссоциации α =0,0132, это означает, что 0,0132 (или 1,32%) общего количества растворённой уксусной кислоты продиссоциировало на ионы, а 0,9868 (или 98,68%) находится в виде недиссоциированных молекул. Диссоциация слабых электролитов в растворе подчиняется закону действия масс.
В общем виде обратимую химическую реакцию можно представить как:
a A + b B D d D + e E
Скорость реакции прямо пропорциональна произведению концентрации реагирующих частиц в степенях их стехиометрических коэффициентов. Тогда для прямой реакции
V 1 =k 1 [A] a [B] b ,
а скорость обратной реакции
V 2 =k 2 [D] d [Е] е.
В некоторый момент времени скорости прямой и обратной реакции выровняются, т.е.
Такое состояние называют химическим равновесием. Отсюда
k 1 [A] a [B] b = k 2 [D] d [Е] е
Сгруппировав постоянные величины с одной стороны, а переменные- с другой стороны, получим:

Таким образом, для обратимой химической реакции в состоянии равновесия произведение равновесных концентраций продуктов реакции в степенях их стехиометрических коэффициентов, отнесенное к такому же произведению для исходных веществ есть величина постоянная при данных температуре и давлении. Численное значение константы химического равновесия К не зависит от концентрации реагирующих веществ. Например, константу равновесия диссоциации азотистой кислоты в соответствии с законом действия масс можно записать в виде:
HNO 2 + H 2 OD H 3 O + + NO 2 -
 .
.
Величину К а называют константой диссоциации кислоты, в данном случае азотистой.
Аналогично выражается и константа диссоциации слабого основания. Например, для реакции диссоциации аммиака:
NH 3 + H 2 O DNH 4 + + OH -
![]() .
.
Величину К b называют константой диссоциации основания, в данном случае аммиака. Чем выше константа диссоциации электролита, тем сильнее электролит диссоциирует и тем выше концентрации его ионов в растворе при равновесии. Между степенью диссоциации и константой диссоциации слабого электролита существует взаимосвязь:
Это математическое выражение закона разбавления Оствальда: при разбавлении слабого электролита степень его диссоциации увеличивается.Для слабых электролитов при К ≤1∙ 10 -4 и С ≥0,1 моль/л используют упрощенное выражение:
К = α 2 ∙С или α
Пример1 . Вычислите степень диссоциации и концентрацию ионов и [ NH 4 + ] в 0,1 М растворе гидроксида аммония, если К NH 4 OH =1,76∙10 -5
Дано: NH 4 OH
К NH 4 OH =1,76∙10 -5
Решение :
Так как электролит является достаточно слабым (К NH 4 OH =1,76∙10 –5 <1∙ 10 - 4) и раствор его не слишком разбавлен, можно принять, что:
 или 1,33%
или 1,33%
Концентрация ионов в растворе бинарного электролита равна C ∙α, так как бинарный электролит ионизирует с образованием одного катиона и одного аниона, то = [ NH 4 + ]=0,1∙1,33∙10 -2 =1,33∙10 -3 (моль/л).
Ответ: α=1,33 %; = [ NH 4 + ]=1,33∙10 -3 моль/л.
Теория сильных электролитов
Сильные электролиты в растворах и расплавах полностью диссоциируют на ионы. Однако экспериментальные исследования электропроводности растворов сильных электролитов показывают, что ее величина несколько занижена по сравнению с той электропроводностью, которая должна бы быть при 100 % диссоциации. Такое несоответствие объясняется теорией сильных электролитов, предложенной Дебаем и Гюккелем. Согласно этой теории, в растворах сильных электролитов между ионами существует электростатическое взаимодействие. Вокруг каждого иона образуется “ионная атмосфера” из ионов противоположного знака заряда, которая тормозит движение ионов в растворе при пропускании постоянного электрического тока. Кроме электростатического взаимодействия ионов, в концентрированных растворах нужно учитывать ассоциацию ионов. Влияние межионных сил создает эффект неполной диссоциации молекул, т.е. кажущейся степени диссоциации. Определенная на опыте величина α всегда несколько ниже истинной α. Например, в 0,1 М растворе Na 2 SO 4 экспериментальная величина α =45 %. Для учета электростатических факторов в растворах сильных электролитов пользуются понятием активности (а). Активностью иона называют эффективную или кажущуюся концентрацию, согласно которой ион действует в растворе. Активность и истинная концентрация связаны между собой выражением:
где f – коэффициент активности, который характеризует степень отклонения системы от идеальной из-за электростатических взаимодействий ионов.
Коэффициенты активности ионов зависят от величины µ, называемой ионной силой раствора. Ионная сила раствора является мерой электростатического взаимодействия всех ионов, присутствующих в растворе и равнаполовине суммы произведений концентраций (с) каждого из присутствующих в растворе ионов на квадрат его зарядового числа (z) :
 .
.
В разбавленных растворах (µ<0,1М) коэффициенты активности меньше единицы и уменьшаются с ростом ионной силы. Растворы с очень низкой ионной силой (µ < 1∙10 -4 М) можно считать идеальными. В бесконечно разбавленных растворах электролитов активность можно заменить истинной концентрацией. В идеальной системе a = c и коэффициент активности равен 1. Это означает, что электростатические взаимодействия практически отсутствуют. В очень концентрированных растворах (µ>1М) коэффициенты активности ионов могут быть больше единицы. Связь коэффициента активности с ионной силой раствора выражается формулами:
![]() при µ
<10 -2
при µ
<10 -2
![]() при 10 -2 ≤ µ
≤ 10 -1
при 10 -2 ≤ µ
≤ 10 -1
![]() + 0,1z 2 µ
при 0,1<µ
<1
+ 0,1z 2 µ
при 0,1<µ
<1
Константа равновесия, выраженная через активности, называется термодинамической. Например, для реакции
a A + b B d D + e E
термодинамическая константа имеет вид:
Она зависит от температуры, давления и природы растворителя.
Поскольку активность частицы , то

где К С - концентрационная константа равновесия.
Значение К С зависит не только от температуры, природы растворителя и давления, но и от ионной силы m . Так как термодинамические константы зависят от наименьшего числа факторов то, следовательно, являются наиболее фундаментальными характеристиками равновесия. Поэтому в справочниках приводятся именно термодинамические константы. Величины термодинамических констант некоторых слабых электролитов приведены в приложении данного пособия. =0,024 моль/л.
С ростом заряда иона коэффициент активности и активность иона уменьшается.
Вопросы для самоконтроля:
- Что такое идеальная система? Назовите основные причины отклонения реальной системы от идеальной.
- Что называют степенью диссоциации электролитов?
- Приведите примеры сильных и слабых электролитов.
- Какая взаимосвязь существует между константой диссоциации и степенью диссоциации слабого электролита? Выразите её математически.
- Что такое активность? Как связаны активность иона и его истинная концентрация?
- Что такое коэффициент активности?
- Как влияет заряд иона на величину коэффициента активности?
- Что такое ионная сила раствора, ее математическое выражение?
- Запишите формулы для расчета коэффициентов активности индивидуальных ионов в зависимости от ионной силы раствора.
- Сформулируйте закон действия масс и выразите его математически.
- Что такое термодинамическая константа равновесия? Какие факторы влияют на ее величину?
- Что такое концентрационная константа равновесия? Какие факторы влияют на ее величину?
- Как связаны термодинамическая и концентрационная константы равновесия?
- В каких пределах могут изменяться величины коэффициента активности?
- В чем заключаются основные положения теории сильных электролитов?
, , 21 , , ,
, 25-26 , 27-28 ,
, 30, , , , , , , , /2003
§ 6.3. Сильные и слабые электролиты
Материал этого раздела частично вам знаком по ранее изученным школьным курсам химии и из предыдущего раздела. Кратко повторим, что вам известно, и познакомимся с новым материалом.
В предыдущем разделе мы обсуждали поведение в
водных растворах некоторых солей и органических
веществ, полностью распадающихся на ионы в
водном растворе.
Имеется ряд простых, но несомненных
доказательств того, что некоторые вещества в
водных растворах распадаются на частицы. Так,
водные растворы серной H 2 SO 4 , азотной HNO 3 ,
хлорной HClO 4 , хлороводородной (соляной) HCl,
уксусной CH 3 COOH и других кислот имеют кислый
вкус. В формулах кислот общей частицей является
атом водорода, и можно предположить, что он (в
виде иона) является причиной одинакового вкуса
всех этих столь различных веществ.
Образующиеся при диссоциации в водном растворе
ионы водорода придают раствору кислый вкус,
поэтому такие вещества и названы кислотами. В
природе только ионы водорода имеют кислый вкус.
Они создают в водном растворе так называемую
кислотную (кислую) среду.
Запомните, когда вы говорите «хлороводород», то имеете в виду газообразное и кристаллическое состояние этого вещества, но для водного раствора следует говорить «раствор хлороводорода», «хлороводородная кислота» или использовать общепринятое название «соляная кислота», хотя состав вещества в любом состоянии выражается одной и той же формулой – НСl.
Водные растворы гидроксидов лития (LiOH), натрия
(NаОН), калия (КОН), бария (Ва(ОН) 2), кальция
(Са(ОН) 2) и других металлов имеют одинаковый
неприятный горько-мыльный вкус и вызывают на
коже рук ощущение скольжения. По-видимому, за это
свойство ответственны гидроксид-ионы ОН – ,
входящие в состав таких соединений.
Хлороводородная HCl, бромоводородная HBr и
йодоводородная HI кислоты реагируют с цинком
одинаково, несмотря на свой различный состав, т.
к. в действительности с цинком реагирует не
кислота:
Zn + 2НСl = ZnСl 2 + Н2,
а ионы водорода:
Zn + 2H + = Zn 2+ + Н 2 ,
и образуются газообразный водород и ионы цинка.
Смешивание некоторых растворов солей, например
хлорида калия KCl и нитрата натрия NaNO 3 , не
сопровождается заметным тепловым эффектом, хотя
после выпаривания раствора образуется смесь
кристаллов четырех веществ: исходных – хлорида
калия и нитрата натрия – и новых – нитрата калия
КNO 3 и хлорида натрия NaCl. Можно предположить,
что в растворе две исходные соли полностью
распадаются на ионы, которые при его выпаривании
образуют четыре кристаллических вещества:
Сопоставляя эти сведения с
электропроводностью водных растворов кислот,
гидроксидов и солей и с рядом других положений,
С.А.Аррениус в 1887 г. выдвинул гипотезу
электролитической диссоциации, согласно которой
молекулы кислот, гидроксидов и солей при
растворении их в воде диссоциируют на ионы.
Изучение продуктов электролиза позволяет
приписать ионам положительные или отрицательные
заряды. Очевидно, если кислота, например азотная
НNO 3 , диссоциирует, предположим, на два иона
и при электролизе водного раствора на катоде
(отрицательно заряженный электрод) выделяется
водород, то, следовательно, в растворе имеются
положительно заряженные ионы водорода Н + .
Тогда уравнение диссоциации следует записать
так:
НNO 3 = Н + + .
Электролитическая диссоциация
–
полный или частичный распад соединения при его
растворении в воде на ионы в результате
взаимодействия с молекулой воды (или другого
растворителя).
Электролиты
– кислоты, основания или
соли, водные растворы которых проводят
электрический ток в результате диссоциации.
Вещества, не диссоциирующие в водном растворе на
ионы и растворы которых не проводят
электрический ток, называются неэлектролитами
.
Диссоциация электролитов количественно
характеризуется степенью диссоциации
– отношением числа распавшихся на ионы
«молекул» (формульных единиц) к общему числу
«молекул» растворенного вещества. Степень
диссоциации обозначается греческой буквой . Например, если из
каждых 100 «молекул» растворенного вещества 80
распадаются на ионы, то степень диссоциации
растворенного вещества равна: = 80/100 = 0,8, или 80%.
По способности к диссоциации (или, как говорят,
«по силе») электролиты разделяют на сильные
,
средние
и слабые
. По степени
диссоциации к сильным электролитам относят те из
них, для растворов которых > 30%, к слабым – < 3%, к средним – 3% 30%. Сила электролита –
величина, зависящая от концентрации вещества,
температуры, природы растворителя и др.
В случае водных растворов
к сильным электролитам
( > 30%) относят
перечисленные ниже группы соединений.
1
. Многие неорганические кислоты,
например хлороводородная НCl, азотная HNO 3 ,
серная H 2 SО 4 в разбавленных растворах.
Самая сильная неорганическая кислота – хлорная
НСlО 4 .
Сила некислородных кислот возрастает в ряду
однотипных соединений при переходе вниз по
подгруппе кислотообразующих элементов:
HCl – HBr – HI.
Фтороводородная (плавиковая) кислота HF растворяет стекло, но это вовсе не говорит о ее силе. Эта кислота из бескислородных галогенсодержащих относится к кислотам средней силы из-за высокой энергии связи Н–F, способности молекул HF к объединению (ассоциации) благодаря сильным водородным связям, взаимодействия ионов F – с молекулами НF (водородные связи) с образованием ионов и других более сложных частиц. В результате концентрация ионов водорода в водном растворе этой кислоты оказывается значительно пониженной, поэтому фтороводородную кислоту считают средней силы.
Фтороводород реагирует с диоксидом кремния, входящим в состав стекла, по уравнению:SiO 2 + 4HF = SiF 4 + 2H 2 O.
Фтороводородную кислоту нельзя хранить в стеклянных сосудах. Для этого используют сосуды из свинца, некоторых пластмасс и стекла, стенки которых покрыты изнутри толстым слоем парафина. Если для «травления» стекла использовать газообразный фтороводород, то поверхность стекла становится матовой, что используется для нанесения на стекло надписей и различных рисунков. «Травление» стекла водным раствором фтороводородной кислоты приводит к разъеданию поверхности стекла, которая остается прозрачной. В продаже обычно бывает 40%-й раствор плавиковой кислоты.
Сила однотипных кислородных кислот изменяется
в противоположном направлении, например йодная
кислота НIО 4 слабее хлорной кислоты НСlО 4 .
Если элемент образует несколько кислородных
кислот, то наибольшей силой обладает кислота, в
которой кислотообразующий элемент имеет самую
высокую валентность. Так, в ряду кислот НСlО
(хлорноватистая) – НСlО 2 (хлористая) – НСlО 3
(хлорноватая) – НСlО 4 (хлорная) последняя
наиболее сильная.
Один объем воды растворяет около двух объемов хлора. Хлор (примерно половина его) взаимодействует с водой:
Cl 2 + H 2 O = HCl + HСlO.
Хлороводородная кислота является сильной, в ее водном растворе практически нет молекул HCl. Правильнее уравнение реакции записать так:
Cl 2 + H 2 O = H + + Cl – + HClO – 25 кДж/моль.
Образующийся раствор называют хлорной водой.
Хлорноватистая кислота – быстродействующий окислитель, поэтому ее применяют для отбеливания тканей.
2 . Гидроксиды элементов главных подгрупп I и II групп периодической системы: LiОН, NaОН, КОН, Са(ОН) 2 и др. При переходе вниз по подгруппе по мере усиления металлических свойств элемента сила гидроксидов возрастает. Растворимые гидроксиды главной подгруппы I группы элементов относят к щелочам.
Щелочами называют растворимые в воде основания. К ним относят также гидроксиды элементов главной подгруппы II группы (щелочно-земельные металлы) и гидроксид аммония (водный раствор аммиака). Иногда щелочами считают те гидроксиды, которые в водном растворе создают высокую концентрацию гидроксид-ионов. В устаревшей литературе вы можете встретить в числе щелочей карбонаты калия К 2 СО 3 (поташ) и натрия Na 2 CO 3 (сода), гидрокарбонат натрия NaHCO 3 (питьевая сода), буру Na 2 B 4 O 7 , гидросульфиды натрия NaHS и калия KHS и др.
Гидроксид кальция Са(ОН) 2 как сильный электролит диссоциирует в одну ступень:
Са(ОН) 2 = Са 2+ + 2ОН – .
3 . Почти все соли. Соль, если это сильный электролит, диссоциирует в одну ступень, например хлорид железа:
FeCl 3 = Fe 3+ + 3Cl – .
В случае водных растворов к слабым электролитам ( < 3%) относят перечисленные ниже соединения.
1 . Вода H 2 O – важнейший электролит.
2
. Некоторые неорганические и почти
все органические кислоты: H 2 S
(сероводородная), H 2 SO 3 (сернистая), H 2 CO 3
(угольная), HCN (циановодородная), Н 3 РО 4
(фосфорная, ортофосфорная), H 2 SiO 3
(кремниевая), H 3 BO 3 (борная, ортоборная),
СН 3 СООН (уксусная) и др.
Заметим, что угольная кислота в формуле H 2 CO 3
не существует. При растворении углекислого газа
СО 2 в воде образуется его гидрат СО 2 Н 2 О,
который мы для удобства расчетов записываем
формулой H 2 CO 3 , и уравнение реакции
диссоциации выглядит так:
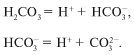
Диссоциация слабой угольной кислоты проходит в
две ступени. Образующийся гидрокарбонат-ион также ведет себя
как слабый электролит.
Точно так же ступенчато диссоциируют и другие
многоосновные кислоты: Н 3 РО 4
(фосфорная), H 2 SiO 3 (кремниевая), H 3 BO 3
(борная). В водном растворе диссоциация
практически проходит лишь по первой ступени. Как
осуществить диссоциацию по последней ступени?
3
. Гидроксиды многих элементов, например
Аl(OH) 3 , Cu(OH) 2 , Fe(OH) 2 , Fe(OH) 3 и др.
Все эти гидроксиды диссоциируют в водном
растворе ступенчато, например гидроксид железа
Fe(OH) 3:
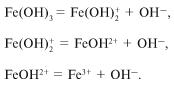
В водном растворе диссоциация проходит
практически только по первой ступени. Как
сместить равновесие в сторону образования ионов
Fe 3+ ?
Осно"вные свойства гидроксидов одного и того же
элемента усиливаются с уменьшением валентности
элемента. Так, осно"вные свойства дигидроксида
железа Fe(OH) 2 выражены сильнее, чем у
тригидроксида Fe(OH) 3 . Это утверждение
равносильно тому, что кислотные свойства Fe(OH) 3
проявляются сильнее, чем у Fe(OH) 2 .
4
. Гидроксид аммония NH 4 OH.
При растворении газообразного аммиака NH 3 в
воде получается раствор, который очень слабо
проводит электрический ток и имеет
горько-мыльный вкус. Среда раствора осно"вная,
или щелочная. Объясняется такое поведение
аммиака следующим образом. При растворении
аммиака в воде образуется гидрат аммиака NH 3 Н 2 О,
которому условно мы приписываем формулу
несуществующего гидроксида аммония NH 4 OH,
считая, что это соединение диссоциирует с
образованием иона аммония и гидроксид-иона ОН – :
NH 4 OH = + ОН – .
5 . Некоторые соли: хлорид цинка ZnCl 2 , тиоцианат железа Fe(NСS) 3 , цианид ртути Hg(CN) 2 и др. Эти соли диссоциируют ступенчато.
К электролитам средней силы некоторые относят фосфорную кислоту Н 3 РО 4 . Мы будем считать фосфорную кислоту слабым электролитом и записывать три ступени ее диссоциации. Серная кислота в концентрированных растворах ведет себя как электролит средней силы, а в очень концентрированных растворах – как слабый электролит. Мы далее будем считать серную кислоту сильным электролитом и записывать уравнение ее диссоциации в одну ступень.